合作客戶/
拜耳公司 |
同濟大學(xué) |
聯(lián)合大學(xué) |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關(guān)新聞Info
-
> 交替型LB膜分析儀有哪些特點呢?
> 溫度對水—十二烷基硫酸鈉體系與純水體系界面張力、厚度的影響——結(jié)果與討論、結(jié)論
> 雙內(nèi)凹結(jié)構(gòu)表面可實現(xiàn)對低表面張力液體的穩(wěn)固超排斥
> 乳膠環(huán)法表面張力儀選型指南
> 去乙酰化槐糖脂生物表面活性劑的結(jié)構(gòu)鑒定、理化性質(zhì)及應(yīng)用(三)
> 堿、表面活性劑濃度變化對三元復(fù)合體系界面張力的影響
> 不同水油黏度比條件下乳化對3種稠油復(fù)合體系的影響(三)
> 不同濃度6∶2氟調(diào)磺酸的表面張力測定儀器及結(jié)果(一)
> 超細纖維:固體表面能的測量過程與操作步驟
> 表面張力的生物醫(yī)學(xué)領(lǐng)域的具體應(yīng)用
推薦新聞Info
-
> 牡蠣低分子肽LOPs雙重乳液制備、界面性質(zhì)檢測及消化吸收特性研究(三)
> 牡蠣低分子肽LOPs雙重乳液制備、界面性質(zhì)檢測及消化吸收特性研究(二)
> 牡蠣低分子肽LOPs雙重乳液制備、界面性質(zhì)檢測及消化吸收特性研究(一)
> 不同水解時間的Protamex酶對玉米谷蛋白表面張力、泡沫、理化性質(zhì)等的影響(三)
> 不同水解時間的Protamex酶對玉米谷蛋白表面張力、泡沫、理化性質(zhì)等的影響(二)
> 不同水解時間的Protamex酶對玉米谷蛋白表面張力、泡沫、理化性質(zhì)等的影響(一)
> 新型納米材料2-D納米黑卡在油水界面的微觀驅(qū)油機理、界面張力測定(三)
> 新型納米材料2-D納米黑卡在油水界面的微觀驅(qū)油機理、界面張力測定(二)
> 新型納米材料2-D納米黑卡在油水界面的微觀驅(qū)油機理、界面張力測定(一)
> 燒結(jié)礦致密化行為研究:不同堿度條件下熔體的表面張力、表觀黏度值(三)
牡蠣低分子肽LOPs雙重乳液制備、界面性質(zhì)檢測及消化吸收特性研究(三)
來源:食品科學(xué)技術(shù)學(xué)報 瀏覽 25 次 發(fā)布時間:2025-07-04
2結(jié)果與分析
2.1 LOPs的界面性質(zhì)分析
2.1.1 LOPs的潤濕性分析
在食品工業(yè)中,濕潤性好的成分可能更容易溶解或分散,從而改善食品的質(zhì)地、口感或加工性能。LOPs(固相)、水(液相)和空氣(氣相)三相之間形成的接觸角θ可用于表示LOPs對水分的親和能力。當(dāng)θ小于90°時,固體顆粒優(yōu)先被水濕潤,θ越小,其在水中的濕潤性及分散性越強;θ大于90°時,固體顆粒的親油性更強;θ在90°左右,固體顆粒具有兩親性,有利于其在界面的吸附與排列。LOPs的固液氣三相接觸角圖片見圖3,LOPs壓片后與超純水和空氣3次接觸形成的接觸角均為銳角,經(jīng)OSA100型全自動界面黏彈性測量儀測得接觸角的平均值為(30.40±3.17)°。隨著時間的延長,最終水滴完全潤濕了LOPs壓片,實驗表明LOPs具有較好的親水性。
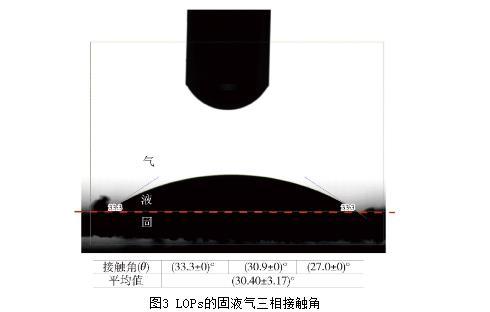
圖3 LOPs的固液氣三相接觸角
2.1.2 LOPs的界面張力分析
蛋白質(zhì)在油水界面的吸附過程分3個階段:擴散、吸附、界面處展開與重排,進而形成蛋白質(zhì)吸附層。這是因為蛋白質(zhì)具有兩親性,疏水側(cè)朝向油相,親水性側(cè)朝向水相,其能夠吸附在油水界面,降低體系自由能和界面張力。同蛋白質(zhì)一樣,經(jīng)酶解獲得的LOPs同樣具有兩親性,其中疏水性氨基酸占氨基酸總量的33.49%,親水性氨基酸占氨基酸總量的57.69%,LOPs的分子質(zhì)量分布在400~2 300 Da,屬于小分子肽。一般認(rèn)為小肽在油水界面具有較快的擴散速率,從而表現(xiàn)出更好的表面活性;也有研究認(rèn)為,較大分子質(zhì)量的肽會優(yōu)先吸附到界面上。
不同質(zhì)量分?jǐn)?shù)的LOPs在油相中的液滴形態(tài)及界面張力變化見圖4。由圖4(a)可以判斷LOPs在純化大豆油中存在擴散過程,且隨著LOPs質(zhì)量分?jǐn)?shù)的增大,液滴的透光性漸無。這可能是因為低質(zhì)量分?jǐn)?shù)的LOPs之間存在親水性氨基酸的互斥作用,從而使得LOPs傾向于擴散至油水界面處,而隨著LOPs質(zhì)量分?jǐn)?shù)的繼續(xù)增加,LOPs持續(xù)擴散至界面處直至體系達到飽和狀態(tài)而失去透光性。由圖4(b)可知,無論LOPs的質(zhì)量分?jǐn)?shù)多大,其在短時間內(nèi)作用于油水間的界面張力無明顯下降,說明短時間內(nèi)LOPs并沒有快速吸附到油水界面,LOPs并沒有降低油水間界面張力的能力。
這可能是由于LOPs表現(xiàn)出強親水性,其中的疏水性氨基酸對大豆油中的酸根離子作用力較小,不足以牽引LOPs分子吸附于界面層,而隨著LOPs濃度的增加,其水溶液在大豆油中的界面張力值越來越小,說明其與大豆油之間的相互作用能降低,更傾向于形成穩(wěn)定的乳液。這可能是因為質(zhì)量分?jǐn)?shù)越大的LOPs分子間作用力越強,并在界面處形成形狀不規(guī)則的肽簇,其中暴露在外的疏水性氨基酸的比例增大。因此,實驗結(jié)果表明,LOPs不具有降低純化大豆油-水間界面張力的能力(乳化能力)。因此,LOPs雙重乳液的構(gòu)建過程中需在中間相(大豆油)添加一定量的乳化劑(PGPR)以形成穩(wěn)定的W1/O乳液。PGPR是一種油溶性表面活性劑,可引起相間油層的結(jié)構(gòu)變化,可促進油相中微小水滴的自發(fā)形成。

圖(a)中液滴下面數(shù)字為LOPs的質(zhì)量分?jǐn)?shù)。
圖4 LOPs水溶液在大豆油中的液滴形態(tài)及界面張力變化
2.2 LOPs雙重乳液體外模擬消化特性分析
2.2.1粒徑分析
在雙乳液遞送系統(tǒng)中,乳液粒徑與分布情況常被用于研究其穩(wěn)定特性。乳液內(nèi)相液滴大小是影響系統(tǒng)穩(wěn)定性的關(guān)鍵因素,內(nèi)相液滴尺寸應(yīng)適當(dāng),數(shù)量多,分布均勻以獲得穩(wěn)定的體系,若液滴尺寸過小,則可能使得液滴之間的碰撞概率增加而破壞乳液的穩(wěn)定性。PDI是衡量顆粒分散均勻性的關(guān)鍵參數(shù),平均粒徑和PDI可反應(yīng)體系的穩(wěn)定程度。LOPs雙重乳液經(jīng)模擬消化后的平均粒徑、PDI和粒徑分布見圖5。由圖5可知,模擬消化前雙重乳液的平均粒徑為(725.5±25.4)nm(PDI=0.419±0.027),顆粒粒徑為1 720 nm的占比最高,達到11.8%。
經(jīng)模擬口腔消化后,乳液的平均粒徑增大為(791.6±20.9)nm(PDI=0.494±0.058),顆粒粒徑為1 990 nm的占比最高,達到15.0%。這可能是模擬唾液中的α-淀粉酶附著在界面膜表面導(dǎo)致乳液的表觀粒徑略微增大,也可能是由于環(huán)境中的OH-附著在界面,與模擬消化液中的鹽離子產(chǎn)生了中和作用,導(dǎo)致乳液的負(fù)電荷量減少,使得液滴間的靜電排斥力減弱而導(dǎo)致液滴聚集。經(jīng)模擬胃液消化后,乳液的平均粒徑顯著增大為(944.6±21.8)nm(PDI=0.418±0.076),此時,顆粒粒徑為1 990 nm的占比仍最高,達到16.2%。以吐溫80為外水相乳化劑制備的LOPs雙重乳液對胃環(huán)境中強酸性、胃蛋白酶、膽鹽和脂肪消化酶有較好的抵抗性,其中吐溫80的聚氧乙烯鏈形成網(wǎng)絡(luò),為膽汁鹽和脂肪酶的吸附提供了空間障礙,吐溫80得以延緩脂質(zhì)的消化。
根據(jù)吐溫80在油水界面的性質(zhì),我們初步判斷LOPs雙重乳液在胃消化中仍能保存良好的界面膜,進而認(rèn)為外界環(huán)境的低滲作用促使水分通過油相中高濃度的PGPR乳化劑形成膠束轉(zhuǎn)移至內(nèi)水相,使得液滴膨脹。此外,胃液中強酸性使得液滴表面質(zhì)子化,而電解質(zhì)的靜電屏蔽作用降低了液滴表面電位,導(dǎo)致液滴聚集在一起,這也可能是模擬胃消化后液滴粒徑增大的原因之一。最后,經(jīng)模擬腸道消化后,乳液的平均粒徑顯著降低為(772.8±21.4)nm(PDI=0.594±0.042),顆粒粒徑為1 990 nm的占比最高,達到11.0%,低于模擬胃消化階段5.2%,說明乳液可能出現(xiàn)破乳現(xiàn)象。
由圖5(b)可知,乳液的粒徑范圍為4 000.0~6 000.0 nm和200.0~400.0 nm的粒徑分布,均大于其他消化階段在此粒徑區(qū)間的粒徑分布。這是因為,隨著模擬消化時間的延長,第一階段的吐溫80對腸道消化液具有抵抗性,體系中液滴的聚集,使得粒徑增大至5 600 nm,而后存在第二階段為膽汁鹽和脂肪酶突破吐溫80的網(wǎng)絡(luò)結(jié)構(gòu),液滴出現(xiàn)破乳現(xiàn)象,進而釋放出W1/O型液滴,并使得乳液的平均粒徑下降。液滴破乳,這可能是由于小分子乳化劑膽鹽對W1/O型液滴中的PGPR乳化劑產(chǎn)生競爭作用,吸附在W1/O液滴界面處,使得胰蛋白酶能夠進一步分解脂肪最終釋放出的LOPs液滴。實驗結(jié)果表明,在整個體外模擬消化過程中,LOPs雙重乳液在口腔和胃腸道消化階段可能出現(xiàn)聚集和膨脹現(xiàn)象而導(dǎo)致表觀粒徑逐漸增大,在腸道消化階段可能出現(xiàn)破乳現(xiàn)象,使得表觀粒徑減小,說明以雙重乳液結(jié)構(gòu)體系輸送的LOPs在胃部消化降解延緩,延續(xù)到小腸消化階段產(chǎn)生破乳降解。
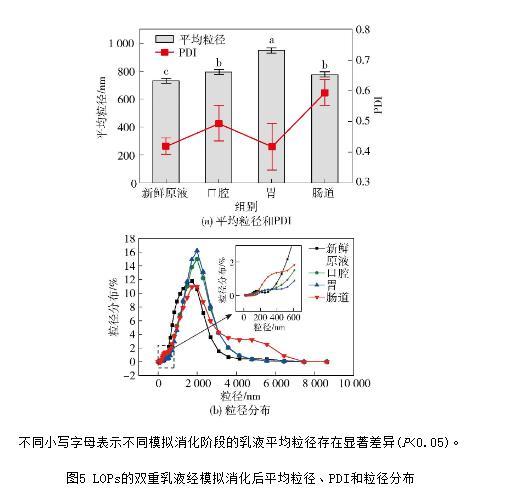
不同小寫字母表示不同模擬消化階段的乳液平均粒徑存在顯著差異(P<0.05)。
圖5 LOPs的雙重乳液經(jīng)模擬消化后平均粒徑、PDI和粒徑分布
2.2.2 LOPs的包封率分析
包封率是生物活性物質(zhì)封裝遞送研究中的指標(biāo)之一,常通過測定內(nèi)相標(biāo)記物的流出率作為評價該系統(tǒng)的封裝效率,以外相標(biāo)記物的流出率評價系統(tǒng)封裝穩(wěn)定性的能力。本研究采用離心法測定內(nèi)水相物質(zhì)LOPs流出率,評價雙重乳液體系在模擬消化階段的封裝效率。LOPs雙重乳液經(jīng)模擬消化后的包封率見圖6。由圖6可知,與消化前乳液相比,經(jīng)模擬口腔消化后LOPs雙重乳液的包封率并無顯著降低(包封率最初為88.35%),說明此階段不存在或存在較少內(nèi)水相物質(zhì)流出,淀粉酶對雙重乳液的影響較小,此時,乳液界面膜結(jié)構(gòu)良好。經(jīng)過模擬胃消化后,乳液的包封率出現(xiàn)顯著性下降,這可能是因為長時間的振蕩作用下,存在內(nèi)水相的LOPs透過界面膜溶出,但乳液仍保留有較高的包封率(76.80%),說明該雙重乳液體系所形成的界面膜結(jié)構(gòu)穩(wěn)定,能抵抗強酸和胃蛋白酶的作用。最后經(jīng)過模擬腸道消化后,乳液的包封率顯著降低(30.01%)。說明經(jīng)過模擬消化過程后,大液滴高度聚集導(dǎo)致界面結(jié)構(gòu)遭到破壞,釋放出內(nèi)部的W1/O型液滴,繼而油相被腸道中的胰酶解離成游離脂肪酸,釋放出內(nèi)部包埋的LOPs。
不同小寫字母表示不同模擬消化階段的包封率存在顯著差異(P<0.05)。
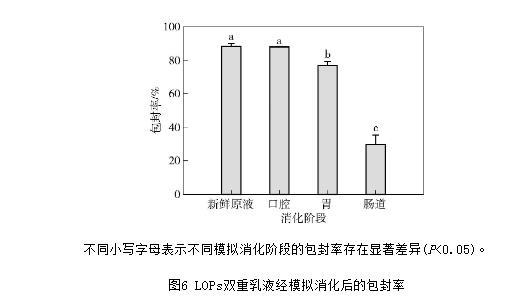
圖6 LOPs雙重乳液經(jīng)模擬消化后的包封率
2.2.3微觀結(jié)構(gòu)分析
圖7是通過光學(xué)顯微鏡拍攝的模擬消化后各階段乳液的形態(tài)。圖7(a)顯示,消化前乳液粒徑大小適宜且分布密集,其中高亮處的乳液粒徑較大,此時乳液具有良好的穩(wěn)定性;圖7(b)顯示,經(jīng)口腔模擬消化后的乳液分布較為稀疏,但仍存在W1/O/W2雙重乳液結(jié)構(gòu);觀察圖7(c),經(jīng)模擬胃消化后的乳液整體粒徑較大且分布相較于圖7(b)密集,同時觀察到中小液滴高密度堆積成帶,說明在強酸和胃蛋白酶存在下,雙重乳液傾向于聚結(jié)在一起,這一結(jié)果增加了液滴間的聚集率,進而導(dǎo)致乳液粒徑增大;圖7(d)結(jié)果顯示,經(jīng)模擬腸道消化后的乳液失去原有的多相結(jié)構(gòu),高度聚結(jié)后的乳液破裂后釋放出W1/O型液滴,又堆積形成大小、形狀不一的大液滴,部分微粒粒徑增大到5 600 nm,而油相經(jīng)膽鹽的乳化作用進一步會形成更小的油滴。實驗結(jié)果表明,經(jīng)模擬口腔、胃消化后的乳液仍具有良好的雙重乳液結(jié)構(gòu),而乳液由于聚集作用,粒徑逐漸增大,最終在模擬腸道消化階段,雙重乳液結(jié)構(gòu)破壞,釋放出的W1/O型乳液在胰酶的作用下分解并釋放出LOPs。
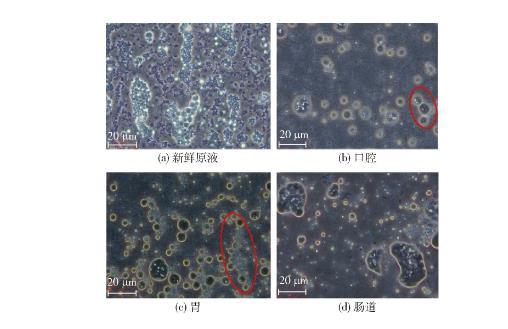
圖(b)中紅圈表示小液滴堆積在大液滴旁邊;圖(c)中紅圈表示小液滴高密度堆積成帶;光學(xué)顯微鏡放大倍數(shù)為(目鏡×物鏡)10×100。
圖7 LOPs的雙重乳液經(jīng)模擬消化后的顯微照片










